Per molte persone che non possono avere figli biologici a causa dell'assenza o della scarsa qualità degli ovuli o dello sperma, le notizie riportate dai giornali su scienziati che producono sperma o ovuli in laboratorio a partire da cellule staminali possono sembrare rivoluzionarie. Ma qual è la scienza che sta dietro a questi titoli e quali sono i limiti per andare avanti? Questa scheda informativa riassume i recenti sviluppi nel trattamento della fertilità e delle malattie genetiche con ovuli e spermatozoi generati da cellule staminali.
Cosa sappiamo?
Le cellule staminali hanno la capacità di svilupparsi in diversi tipi di cellule quando ricevono le giuste istruzioni. Alcune cellule staminali possono dare origine a qualsiasi tipo di cellula del corpo. Queste sono chiamate pluripotenti.
Le cellule staminali pluripotenti possono essere ricavate a partire da embrioni di cinque giorni, prima che l'embrione si impianti nell'utero. Queste cellule (note come cellule staminali embrionali o ESC) possono essere coltivate in laboratorio in grandi quantità, mantenendo la loro capacità di differenziarsi in altri tipi di cellule.
Le cellule staminali pluripotenti possono anche essere generate “riprogrammando” altre cellule del corpo in laboratorio, come ad esempio le cellule della pelle (queste sono note come cellule staminali pluripotenti indotte, o iPSC).
Queste cellule staminali suscitano particolare interesse per il potenziale utilizzo in trattamenti di fertilità, poiché gli scienziati potrebbero essere in grado di utilizzare cellule staminali pluripotenti per produrre spermatozoi e ovuli (chiamati collettivamente gameti) destinati alla fecondazione in vitro. Il processo di creazione di spermatozoi e ovuli in laboratorio è chiamato gametogenesi in vitro o IVG.
Sebbene siano già stati ottenuti topi a partire da ovuli e spermatozoi derivati da cellule staminali e IVG, questo risultato non è ancora stato raggiunto nell’uomo.
A cosa stanno lavorando i ricercatori?
La ricerca in corso è diretta a diversi aspetti dell'IVG.
- Alcuni gruppi stanno sviluppando nuovi metodi per produrre cellule precursori di ovuli e spermatozoi (cellule germinali primordiali, o PGC) a partire da cellule staminali pluripotenti umane, e stanno poi studiando come indirizzarle verso lo sviluppo in spermatozoi o ovuli.
- Altri gruppi stanno cercando di ricreare in laboratorio un ambiente favorevole in cui queste cellule precursori possano svilupparsi in spermatozoi o ovuli, il che significa riprodurre il testicolo o l'ovaio in fase di sviluppo. Questo processo comporta l'induzione delle cellule staminali a differenziarsi in altri tipi di cellule del testicolo (come le cellule di Sertoli, che supportano lo sviluppo delle PGC, o le cellule di Leydig, produttrici di testosterone) o dell'ovaio (come le cellule della granulosa, che supportano la maturazione degli ovuli).
- Questi metodi vengono utilizzati anche per comprendere le condizioni in cui lo sviluppo dei testicoli o delle ovaie risulta compromesso, con possibili ripercussioni sulla fertilità o sulle caratteristiche sessuali. Questo tipo di ricerca è chiamata modellizzazione delle malattie e può includere lo studio dei geni coinvolti nelle diverse fasi della formazione di ovaie e testicoli funzionali, nonché di ovuli e spermatozoi.
Quali sono le sfide?
Se fosse possibile produrre ovuli e spermatozoi da altri tipi di cellule adulte attraverso l’IVG, questa tecnologia potrebbe avere ampie applicazioni per le persone affette da infertilità o a rischio di trasmettere malattie genetiche. Tuttavia, attualmente esistono quattro principali ostacoli che limitano l'applicazione delle tecnologie IVG negli esseri umani:
- Produrre un numero sufficiente di cellule precursori di ovuli e spermatozoi (PGC) a partire da cellule staminali.
- Garantire che queste PGC umane producano ovuli e spermatozoi senza dare origine a tumori, un rischio associato alle cellule pluripotenti.
- Capire come far maturare le PGC umane in ovuli e spermatozoi completamente funzionali in laboratorio, evitando così il trapianto di PGC immature nelle persone. Ciò eliminerebbe le procedure invasive e preverrebbe il rischio di formazione di tumori.
- Stabilire in che modo valutare se lo sperma e gli ovuli generati in laboratorio siano capaci di dare origine a embrioni e bambini sani, tenendo conto delle attuali restrizioni, presenti in molti Paesi, circa la creazione di embrioni per la ricerca o sulla loro coltura in laboratorio oltre determinati stadi di sviluppo.
Oltre al superamento delle sfide scientifiche, i prossimi passi dovranno tenere conto anche delle significative barriere sociali, etiche e legali legate all'uso dell'IVG. Le normative che disciplinano l'uso e la generazione di embrioni differiscono da Paese a Paese. Se le tecnologie di IVG diventassero scientificamente concrete, sarà necessario modificare la legislazione per consentirne l'applicazione clinica.
Introduzione alle tecnologie di riproduzione assistita
Le tecnologie di procreazione medicalmente assistita (PMA) sono tecnologie che aiutano le coppie o gli individui a ottenere una gravidanza senza ricorrere al rapporto sessuale. Ciò comporta la manipolazione di spermatozoi, ovuli o embrioni al di fuori del corpo umano. Le procedure PMA comprendono l'uso della fecondazione in vitro (FIV), in cui gli embrioni vengono creati in laboratorio e poi trasferiti nell'utero della madre intenzionale o di una madre surrogata. Le PMA possono anche prevedere l'uso di gameti donati (spermatozoi o ovuli) o di embrioni già fecondati.
Le PMA possono essere utilizzate per diversi motivi:
- Infertilità: l'Organizzazione Mondiale della Sanità riporta che un adulto su sei soffre di infertilità e potrebbe quindi non essere in grado di concepire. L'infertilità può essere causata da una serie di condizioni e fattori e può colpire qualsiasi individuo.
- Uso di gameti donati: le persone che sperimentano problemi di infertilità, le coppie dello stesso sesso o chi desidera concepire e crescere un figlio da solo possono scegliere di utilizzare gameti donati da terzi.
- Rischi genetici noti: se uno o entrambi i genitori sanno di essere portatori di una malattia genetica che riduce l'aspettativa di vita, possono scegliere di concepire tramite FIV e sottoporsi a test genetici preimpianto. Questo processo consente di analizzare gli embrioni e selezionare per l’impianto quelli che non presentano la mutazione genetica, in modo da evitare che la trasmissione della malattia genetica specifica dei genitori al bambino.
Trattamenti e supporto attuali
Per le persone o le coppie con problemi di fertilità o che non riescono a concepire, le tecniche di PMA, compresa la fecondazione in vitro (FIV), consentono la fecondazione degli ovuli con gli spermatozoi in laboratorio. Gli ovuli maturi vengono prelevati dalle ovaie; ciò prevede l'uso di farmaci che sopprimono il ciclo mestruale naturale e combinazioni di ormoni per stimolare la maturazione delle cellule uovo. Una volta raccolti, gli ovuli vengono fecondati con gli spermatozoi in laboratorio.
Gli embrioni ottenuti vengono coltivati per un massimo di 6 giorni e ne viene valutato lo sviluppo. A questo punto, se uno dei genitori è portatore di una patologia genetica che riduce le aspettative di vita, può richiedere un test genetico preimpianto, che consente di analizzare in laboratorio il patrimonio genetico dell'embrione. Gli embrioni privi della mutazione responsabile della malattia vengono identificati, in modo da evitarne la trasmissione al bambino. Gli embrioni possono quindi essere trasferiti nell'utero della madre intenzionale o di unasurrogata, oppure congelati e conservati per un utilizzo futuro.
Tuttavia, affinché le attuali tecnologie di PMA portino alla nascita di un embrione biologicamente correlato, è necessario che almeno uno dei genitori disponga di gameti vitali.
Per le persone e le coppie che non possiedono spermatozoi o ovuli idonei, possono essere utilizzati gameti o embrioni donati. Ciò implica che il bambino che ne nascerà non sarà geneticamente imparentato con uno o entrambi i genitori intenzionali. L'accesso a gameti o embrioni donati può risultare complesso a causa delle limitazioni e restrizioni legate alla donazione, nonché dal numero limitato di donatori.
Attualmente, le alternative alla PMA sono l'adozione e la scelta di non avere figli.
In che modo le terapie geniche e cellulari possono essere d'aiuto?
Per creare un embrione biologicamente correlato, le PMA esistenti richiedono che almeno uno dei genitori disponga di ovuli o spermatozoi sani e funzionali. Tuttavia, i ricercatori stanno studiando come produrre ovociti e spermatozoi sani a partire da cellule staminali in laboratorio (un processo chiamato gametogenesi in vitro o IVG), ma questo risultato non è ancora stato ottenuto nell'uomo.
Ci sono diversi motivi per cui un individuo o una coppia potrebbero trarre beneficio dall'IVG:
- Quando le tecniche di PMA già esistenti non hanno avuto successo.
- Quando le tecniche di PMA esistenti non sono praticabili, a causa della mancanza di ovaie/testicoli, ovuli/spermatozoi oppure di infertilità dovuta all'età o a trattamenti oncologici.
- Quando entrambi i partner sono portatori di una malattia genetica e desiderano creare un numero più ampio di embrioni tra cui scegliere.
- Per evitare i rischi e gli oneri delle attuali tecniche di PMA, che possono includere iniezioni ormonali, monitoraggio frequente e prelievo degli ovuli.
- Per coppie dello stesso sesso, che producono naturalmente solo ovuli o sperma.
- Per persone single sterili che desiderano creare un ovulo o uno spermatozoo dalle proprie cellule staminali da fecondare con un gamete donato.
- Per persone single che desiderano utilizzare il proprio ovulo o sperma naturale insieme a un gamete derivato dalle proprie cellule staminali, consentendo loro di diventare l'unico genitore genetico.
Cosa sono le cellule staminali pluripotenti?
Le cellule staminali pluripotenti sono cellule che possono diventare qualsiasi altro tipo di cellula dell’organismo. Durante lo sviluppo dell'embrione, le popolazioni di cellule staminali si differenziano nei vari tipi cellulari, perdendo la loro pluripotenza. Tuttavia, esistono metodi che consentono di “riprogrammare” una cellula matura riportandola ad uno stato pluripotente; queste cellule pluripotenti (iPSC) possono quindi dare origine a qualsiasi tipo di cellula del corpo.
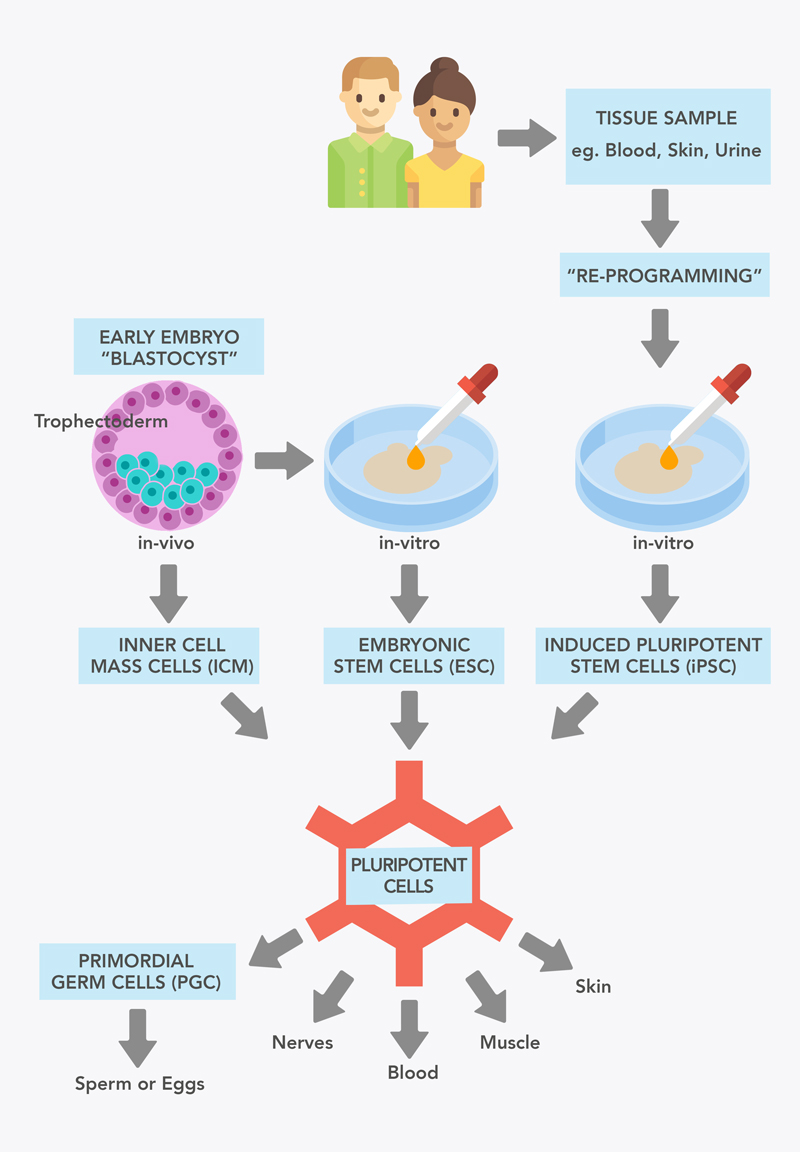
Figura 1: Fonti di cellule staminali pluripotenti.
Un tipo di cellula staminale pluripotente può essere ottenuto da uno stadio molto precoce dello sviluppo embrionale. A cinque giorni, l'embrione è chiamato blastocisti. Questa è costituita da uno strato esterno di cellule, chiamato trofoblasto, e da uno strato interno, chiamato massa cellulare interna (ICM). Le cellule dell'ICM sono pluripotenti, ma dopo l'impianto nell'utero si differenziano per formare le cellule e i tessuti embrionali.
Quando le cellule pluripotenti dell'ICM vengono coltivate al di fuori dell'embrione in laboratorio, vengono definite cellule staminali embrionali (ESC). Le ESC sono state il primo tipo di cellule staminali pluripotenti (PSC) a disposizione dei ricercatori. Sono state ottenute per la prima volta da embrioni umani nel 1998.
Non esistono fonti consolidate di cellule staminali pluripotenti nei bambini o negli adulti, poiché la maggior parte delle loro cellule ha già un destino cellulare prestabilito.
Tuttavia, nel 2006,However, in 2006, il ricercatore Shinya Yamanaka ha dimostrato che anche le cellule della pelle di topo potevano essere indotte a diventare cellule staminali pluripotenti. Questo processo è noto come “riprogrammazione”. Queste cellule assomigliavano alle cellule staminali embrionali e sono state denominate cellule staminali pluripotenti indotte (iPSC). Come le cellule staminali embrionali, anche queste cellule hanno il potenziale di differenziarsi in tutti i tipi di cellule del corpo, compresi, potenzialmente, ovuli e spermatozoi. Ben presto questa tecnologia si è dimostrata efficace anche per le cellule umane. La generazione di iPSC ha rivoluzionato il campo delle cellule staminali e la medicina in generale, e nel 2012 , è stata insignita del Premio Nobel, a soli cinque anni dalla sua applicazione alle cellule umane. Oggi, le cellule staminali pluripotenti indotte sono state prodotte da diversi tipi di cellule, tra cui cellule della pelle, del sangue e persino cellule raccolte dalle urine.
Utilizzo di cellule staminali pluripotenti per produrre spermatozoi e ovuli sani
Nei topi, le cellule staminali pluripotenti sono state utilizzate per produrre spermatozoi e ovuli a partire da cellule di topo. Negli esseri umani, invece, non è stato possibile produrre ovuli e spermatozoi a partire da cellule staminali pluripotenti, sebbene siano stati fatti progressi nella produzione delle cellule precursori (cellule germinali primordiali, PGC).
I ricercatori giapponesi Katsuhiko Hayashi e Mitinori Saitou sono stati i pionieri della tecnologia della gametogenesi in vitro (IVG) utilizzando modelli animali. Nel 2011 hanno dimostrato che le PSC di topo potevano essere riprogrammate per diventare spermatozoi, capaci di svilupparsi in cuccioli sani e fertili. L'anno successivo, hanno dimostrato che le PSC femminili di topo potevano essere indotte a formare ovuli, anch'essi in grado di svilupparsi in cuccioli sani e fertili.
Diversi fattori sono stati fondamentali per questo successo:
Several factors were critical to this success:
- Il tipo di cellula di partenza: dopo l'impianto dell'embrione, la massa cellulare interna si trasforma in cellule “dell’epiblasto”. Alcune di queste cellule escono dall'embrione in via di sviluppo e diventano cellule germinali primordiali (PGC). Successivamente, queste PGC migrano nel feto e si insediano nelle ovaie o nei testicoli in formazione, dove si trasformano rispettivamente in ovuli o spermatozoi. Alcuni ricercatori hanno cercato di produrre cellule simili a quelle dell’epiblasto. Tuttavia, Hayashi e colleghi hanno dimostrato che queste cellule non erano molto efficaci nel generare PGC. In alternativa, hanno sviluppato un nuovo tipo di cellula epiblastica a partire dalle ESC di topo: la cellula epiblasto-simile (epiblast-like cell). Questo tipo cellulare ha avuto più successo nel formare PGC e, successivamente, ovuli e spermatozoi.
- Purezza del tipo cellulare: quando si differenziano cellule staminali pluripotenti in tipi cellulari specifici, è difficile che tutte le cellule rispondano esattamente allo stesso modo. Ciò può portare a una popolazione cellulare mista, comprendente tipi non desiderati o cellule che mantengono la pluripotenza e non riescono a formare ovuli e spermatozoi. Queste cellule possono anche dare origine a tumori. La purificazione delle PGC è fondamentale per rimuovere i tipi cellulari indesiderati, e questi studi hanno sviluppato metodi per farlo.
- Un requisito per la maturazione in vivo: in questi studi, il processo di produzione di ovuli e spermatozoi funzionali e maturi ha richiesto il trapianto delle cellule simili alle PGC rispettivamente nelle ovaie o nei testicoli dei topi. In questo ambiente, le cellule ricevono il supporto per svilupparsi ulteriormente fino a diventare ovuli e spermatozoi, un risultato che all'epoca non era stato ancora ottenuto in laboratorio. Capire come l'ovaio/testicolo supporti questa maturazione è importante: ciò consentirà ai ricercatori di ricreare queste condizioni in laboratorio, eliminando la necessità di procedure invasive e rischiose o di testicoli e ovaie funzionali.
Ulteriori ricerche hanno continuato a migliorare questa tecnologia. Nel 2016, Saitou e Hayashi hanno dimostrato che le ESC e le iPSC di topo potevano essere sviluppate in ovuli maturi in vitro, senza la necessità di reimpiantarle nelle ovaie dei topi per completare la maturazione. Tuttavia, era ancora necessario utilizzare il tessuto ovarico prelevato dai topi per sostenere lo sviluppo degli ovuli.
Da allora, la necessità di tessuto ovarico di topo è stata recentemente superata grazie al lavoro del laboratorio di Hayashi, che ha creato cellule di supporto ovariche a partire cellule staminali. Queste cellule sono state in grado di sostenere lo sviluppo di cellule simili alle PGC, derivate da cellule staminali, in ovuli vitali, che potevano essere fecondati e dare origine a embrioni vitali.
Analogamente, il lavoro del laboratorio di Zhou in Cina ha dimostrato la creazione di cellule simili a precursori degli spermatozoi da ESC di topo, senza la necessità di tessuto testicolare, consentendo, per la prima volta, una IVG completa senza la necessità di tessuto proveniente da un modello animale.
E negli esseri umani?
Alcuni ricercatori hanno cercato di ricreare questi risultati utilizzando cellule umane, ma finora non sono stati in grado di produrre spermatozoi o ovuli funzionali da cellule staminali umane. Ci sono ancora delle lacune nella nostra comprensione dello sviluppo embrionale umano naturale. Dal primo successo nella produzione di cellule simili alle PGC da cellule staminali umane in vitro, diversi gruppi di ricerca hanno sviluppato metodi più efficienti o raffinati per produrre i precursori dei gameti. Tuttavia, la maturazione di questi in ovuli e spermatozoi funzionali rimane una sfida.
Nel 2018, Yamashiro e colleghi hanno creato cellule che assomigliano alle cellule uovo umane nelle fasi iniziali di sviluppo a partire da iPSC. Tuttavia, per questo processo si sono basati sull'uso di tessuto ovarico di topo per sostenere il differenziamento delle cellule. Analogamente, nel 2021, Hwang e colleghi hanno derivato cellule precursori dello sperma umano da iPSC, ma anche in questo caso hanno utilizzato cellule testicolari di topo per sostenerne lo sviluppo.
Test genetici preimpianto
Gli individui o le coppie che sanno di essere portatori di una malattia genetica potrebbero voler evitare di trasmetterla ai propri figli. Attualmente, esiste un solo modo per evitare attivamente l'impianto di un embrione portatore della malattia genetica: il test genetico preimpianto (PGT), che può essere utilizzato solo in combinazione con la FIV.
Dopo che gli embrioni sono stati fecondati in clinica per FIV, vengono coltivati per alcuni giorni, fino a raggiungere lo stadio di blastocisti, costituito dalla massa cellulare interna e dal trofoectoderma circostante. Il trofoectoderma è costituito dalle cellule che, durante la gravidanza, formano strutture di supporto come la placenta e le membrane amniotiche. A questo stadio, i genitori possono optare per il PGT.
Dal trofoectoderma vengono prelevate 4-5 cellule. Queste cellule vengono sequenziate geneticamente per individuare la variante responsabile della malattia. Gli embrioni che non presentano la mutazione genetica vengono identificati e possono essere trasferiti nell'utero della madre intenzionale o della madre surrogata, oppure congelati per uso futuro. Questo processo riduce il numero di embrioni utilizzabili da una coppia e può quindi richiedere un numero maggiore di embrioni di partenza. In alcuni casi, sono necessari più cicli di FIV prima di ottenere una gravidanza con un embrione privo di varianti genetiche. Non è possibile testare geneticamente gli ovuli e gli spermatozoi prima della fecondazione, poiché le tecniche attuali di analisi del DNA cellulare distruggerebbe la cellula.
È stato proposto che l'editing genico potrebbe essere potenzialmente utilizzato per correggere le mutazioni negli embrioni analizzati, anziché selezionare quelli senza mutazioni. Tuttavia, esistono importanti considerazioni tecniche ed etiche che lo impediscono. La tecnologia di editing genico attualmente disponibile può influenzare parti non mirate del DNA, causando effetti collaterali indesiderati. Inoltre, sarebbe difficile correggere la mutazione in tutte le cellule dell'embrione, con il rischio che alcune cellule restino portatrici della mutazione compromettendo la salute del bambino.
La produzione di ovuli e spermatozoi a partire da cellule staminali pluripotenti potrebbe rappresentare un'alternativa al tentativo di modificare i geni direttamente in un embrione. Questo perché la variante genetica potrebbe essere corretta nelle cellule staminali prima che queste vengano utilizzate per generare i gameti. La correzione delle varianti genetiche nelle cellule staminali è una tecnologia già consolidata. Le cellule possono quindi essere sottoposte a screening per individuare mutazioni non desiderate, prima di produrre ovuli o spermatozoi. Inoltre, poiché le cellule staminali possono essere facilmente coltivate in grandi quantità, sarebbe possibile produrre un numero di gameti superiore a quello che normalmente verrebbe raccolto in un ciclo di FIV. Di seguito sono riportati alcuni esempi di come sia possibile evitare l'ereditarietà delle malattie genetiche.
- Modifica del genoma CRISPR/Cas9: il codice del DNA delle cellule staminali potrebbe essere modificato. Ciò potrebbe significare aggiungere una parte “mancante”, rimuovere una parte che codifica un gene associato ad una patologia, oppure correggere una variante genetica in modo che codifichi correttamente per un gene sano. Le cellule corrette verrebbero quindi selezionate e fatte crescere. Ciò significherebbe che tutti gli ovuli e gli spermatozoi ottenuti da queste cellule staminali corrette non sarebbero portatori della variante responsabile della malattia. Prima della produzione di ovuli e sperma, potrebbero anche essere testate le mutazioni indesiderate (off-target).
- Selezione: per le patologie causate dal mosaicismo (condizioni in cui una variazione genetica si riscontra solo in alcune cellule), è possibile identificare e isolare singole cellule staminali pluripotenti che non portano la mutazione che causa la malattia. Queste cellule potrebbero quindi essere coltivate per la produzione di ovuli e spermatozoi.
- Rimozione dei cromosomi in eccesso: alcune condizioni che influenzano la fertilità sono causate daaneuploidie cromosomiche, in cui un individuo possiede un numero superiore o inferiore di cromosomi. In questo caso, le cellule staminali potrebbero essere utilizzate anche per produrre gameti privi di aneuploidia. Nei topi, gli scienziati sono riusciti a rimuovere con successo i cromosomi in eccesso dalle cellule pluripotenti e a utilizzarle per generare cuccioli sani. Altri hanno anche alterato il numero di cromosomi in modelli di cellule iPSC umane per la sindrome di Down (trisomia 21, in cui un cromosoma 21 in eccesso causa una serie di problemi tra cui l'infertilità) e per la sindrome di Klinefelter (dove gli individui hanno cromosomi XXY). Ciò potrebbe essere applicato ad altri disturbi umani causati dalla presenza di cromosomi in eccesso. Una tecnologia simile potrebbe potenzialmente essere utilizzata per individui che producono ovuli o spermatozoi con aggiunta o rimozione sporadica di cromosomi, un fenomeno che aumenta con l'invecchiamento.
Prossimi passi
Attualmente, ci sono quattro principali ostacoli da superare prima di poter applicare all’uomo il processo utilizzato negli studi sui topi:
Nel 2015, uno studio britannico sull'uomo è riuscito a produrre PGC con un'efficienza piuttosto elevata, senza utilizzare tessuti di supporto; circa il 40% delle cellule si è sviluppato in cellule simili alle PGC. I ricercatori ritengono inoltre di aver trovato un modo per purificare questa popolazione di cellule simili alle PGC umane, al fine di evitare la formazione di tumori. Questo studio rappresenta un passo avanti verso la risoluzione degli ostacoli 1 e 2. Tuttavia, non sono stati riportati tentativi per far maturare o trapiantare queste cellule.
Altri laboratori stanno lavorando per generare le cellule somatiche di supporto dei testicoli o delle ovaie, e persino alla creazione di replicati 3D in vitro dei tessuti ovarici o testicolari (chiamati organoidi) derivati interamente da cellule staminali. Questo potrebbe essere necessario per produrre gameti completamente funzionali in vitro, e potrebbe essere utilizzato anche per molte altre applicazioni della medicina riproduttiva come lo screening di farmaci, la modellizzazione di malattie e la valutazione dell'impatto degli inquinanti ambientali.
Affrontare le sfide legali, etiche e sociali
Oltre a superare le barriere scientifiche, i prossimi passi devono includere anche la considerazione delle significative barriere sociali, etiche e legali. La legislazione che disciplina l'uso e la creazione di embrioni varia in tutto il mondo e spesso riflette la cultura e gli standard sociali unici di ciascun Paese, nonché la legislazione esistente per aree simili di ricerca e medicina. Se le tecnologie IVG diventeranno scientificamente fattibili, la legislazione dovrà essere modificata per consentirne l'applicazione clinica. Qualsiasi riforma normativa sarà probabilmente influenzata dall'opinione della comunità sull'IVG e sulle tecnologie riproduttive, e in particolare dal modo in cui saranno affrontate le principali considerazioni etiche, quali: chi dovrebbe avere diritto a utilizzare queste tecnologie, come sarà garantito un accesso equo alle tecnologie e, soprattutto, quali misure di sostegno saranno messe in atto per monitorare adeguatamente nel corso del tempo la salute dei bambini eventualmente nati
È possibile produrre ovuli da cellule staminali maschili o spermatozoi da cellule staminali femminili in provettavitro?
Attualmente non ci sono prove che nell'uomo l'IVG possa essere utilizzata per creare spermatozoi da cellule staminali femminili o ovuli da cellule staminali maschili. Tuttavia, ricerche condotte sui topi forniscono prove che ciò potrebbe essere possibile.
Quali prove abbiamo a favore o contro questa possibilità?
Prove della produzione di ovuli da cellule staminali pluripotenti XY (maschili) o di spermatozoi da cellule staminali pluripotenti XX (femminili):
Nel 2018, Li e colleghi hanno creato topi vivi con due madri (bimaterni) e topi vivi con due padri (bipaterni). Tuttavia, i topi bipaterni non erano vitali a lungo termine, poiché morivano poco dopo la nascita.
Nel 2023, Murakami e colleghi sono riusciti a convertire cellule staminali XY (maschili) in cellule staminali XX (femminili). Queste cellule staminali XY --> XX hanno poi prodotto ovuli maturi e funzionali con la stessa efficienza delle cellule staminali XX naturali. Una volta fecondati, questi ovuli hanno dato origine a prole viva, fornendo così prova della riproduzione bipaterna nei topi.
Prove contro la produzione di ovuli da cellule XY (maschili) o di sperma da cellule XX (femminili):
Mentre l'articolo del 2023 di Murakami e colleghi indica che ciò potrebbe essere possibile, decenni di precedenti ricerche sulla formazione dei gameti nei mammiferi e sulla determinazione del sesso avevano messo in dubbio la possibilità di formare ovuli da cellule con cromosomi XY o spermatozoi da cellule prive di essi (come discusso in Taketo 2015). Questi studi precedenti sostengono che la produzione di spermatozoi da cellule XX (femminili) o di ovuli da cellule XY (maschili) non fosse possibile. Inoltre, la barriera allo sviluppo di individui sani è riscontrabile nelle aneuploidie dei cromosomi sessuali umani associate alla sterilità, tra cui:
- Femmine XY - Sindrome di Swyer
- Maschi XX - Sindrome di de la Chapelle
- Maschi XXY - Sindrome di Klinefelter
- Femmine XO - Sindrome di Turner
È importante notare che la maggior parte di questi studi esamina condizioni in cui sia gli ovuli o gli spermaozoi, sia l'ambiente di supporto delle ovaie o dei testicoli, presentano anomalie genetiche. Non sono ancora stati condotti esperimenti che prevedono l'inserimento di PGC XY sane in un ovaio XX sano, o di PGC XX sane in un testicolo XY sano. Tuttavia, tali esperimenti sarebbero teoricamente possibili utilizzando i metodi Hayashi discussi sopra.
Saranno necessarie ulteriori ricerche per verificare se il lavoro di Murakami e colleghi possa essere ripetuto in modo affidabile.
